Интересные факты
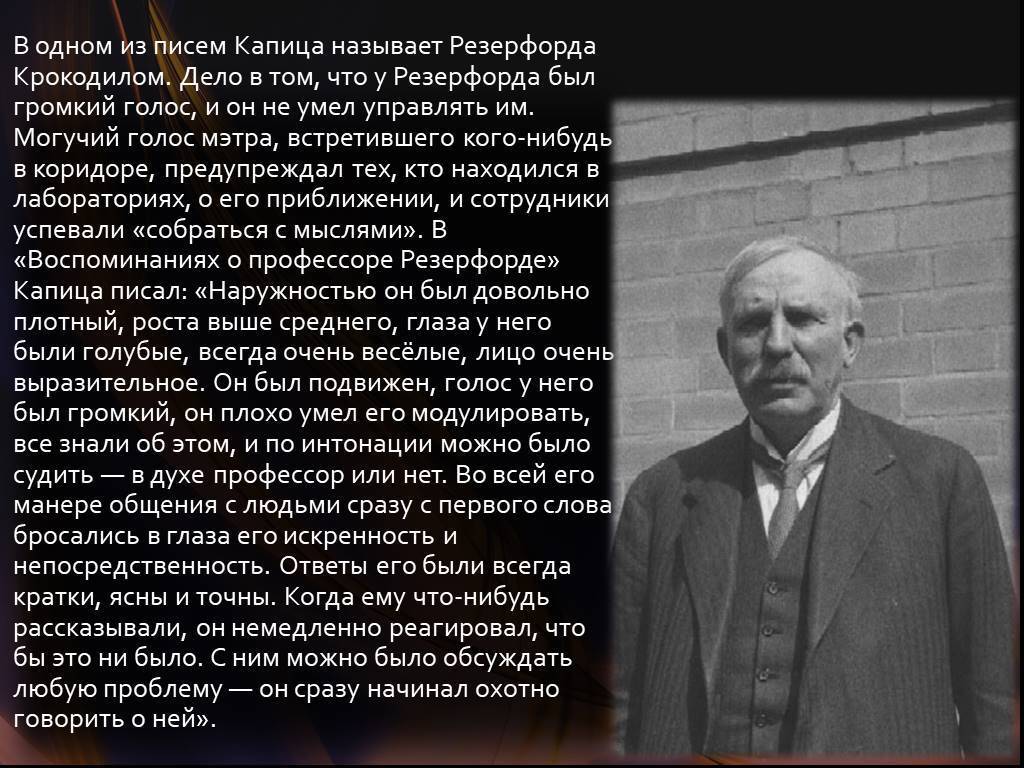
По словам Ива, Капица так объяснял придуманное им прозвище: «Это животное никогда не поворачивает назад и потому может символизировать Резерфордовскую проницательность и его стремительное продвижение вперед». Капица добавлял, что «в России на Крокодила смотрят со смесью ужаса и восхищения». В советских биографических очерках существует другая версия: «Дело в том, что у Резерфорда был громкий голос и он не умел управлять им. Могучий голос метра, встретившего кого-нибудь в коридоре,предупреждал тех, кто находился в лабораториях, о его приближении, и сотрудники успевали “собраться с мыслями”. Это дало Капице основание прозвать Резерфорда Крокодилом. Объясняют это ассоциацией с героем популярной детской книжки Крокодилом, который проглотил будильник. Его тиканье предупреждало детей о приближении страшного зверя.» (Ф. Кедров. Капица: жизнь и открытия. М.: Московский рабочий. 1979)
- Э. Резерфорд, открывший ядро атома, негативно отзывался о перспективах ядерной энергетики: «Каждый, кто надеется, что преобразования атомных ядер станут источником энергии, исповедует вздор».
- Когда Пётр Капица приехал работать в Кембридж к Резерфорду, то он ему сказал, что штат лаборатории уже укомплектован. Тогда Капица спросил:
- — Какую допустимую погрешность вы допускаете в экспериментах?
- — Обычно около 3 %.
- — А сколько человек работает в лаборатории?
- — 30.
- — Тогда 1 человек составляет примерно 3 % от 30.
- Резерфорд рассмеялся и принял Капицу в качестве «допустимой погрешности». В действительности же Капицу взяли в лабораторию благодаря рекомендации физика Иоффе[источник не указан 2254 дня].
Получив в 1908 году известие о присуждении ему Нобелевской премии по химии, Резерфорд заявил: «Вся наука — или физика, или коллекционирование марок». (All science is either physics or stamp collecting.)
Опыты Резерфорда
В 1913 г. английский физик Резерфорд проделал классические опыты по рассеянию a-частиц тонкими слоями различных веществ. a-частицы, испускаемые радиоактивными веществами, являются подходящими пробными зарядами для исследования внутриатомных электрических полей. Они представляют собой полностью ионизированные атомы гелия, имеют положительный заряд, равный удвоенному элементарному заряду (q = 3.2·10-19 Кл), массу m = 6.67·10-27кг, обладают высокой энергией (а значит и скоростью), достаточной для проникновения в атомы вещества.
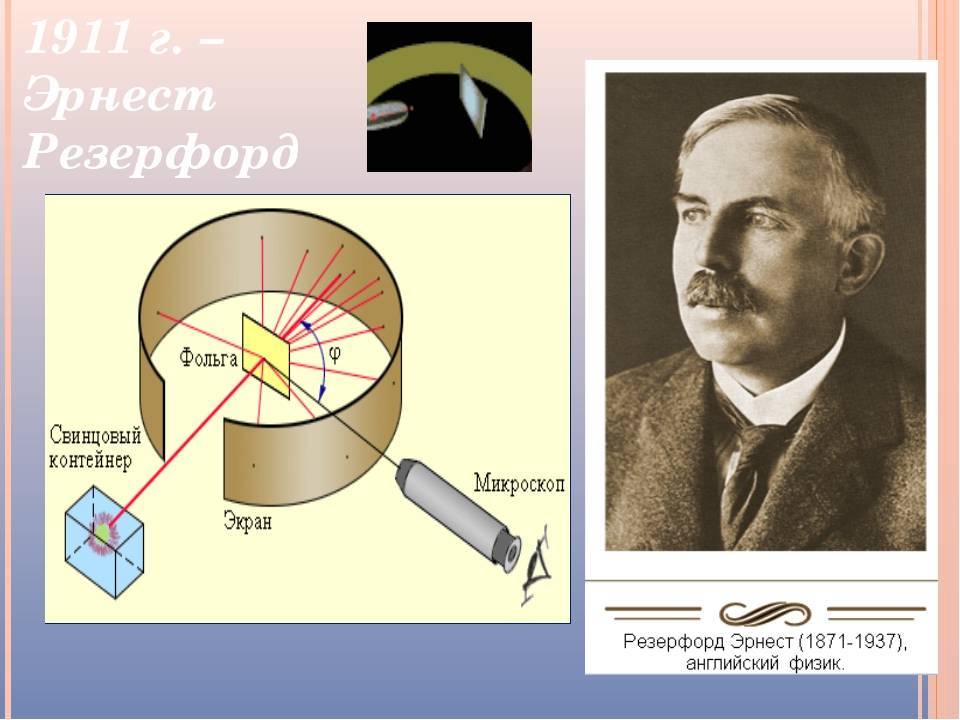
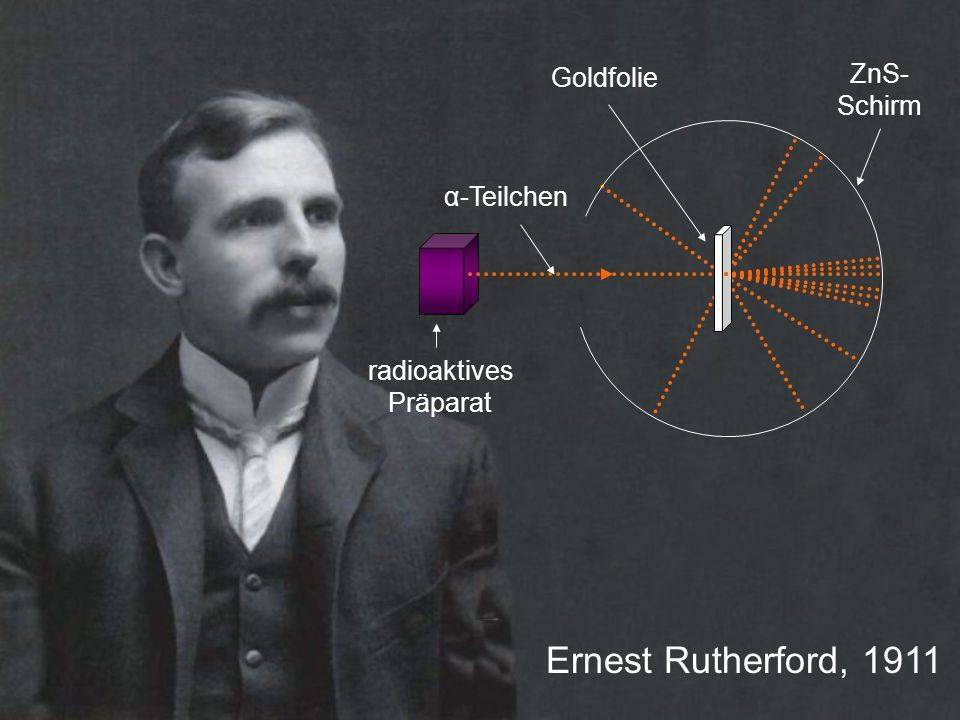
Схема опытов Резерфорда и его учеников Гейгера и Марсдена изображена на рис.1.Внутри герметичной камеры, в которой был создан высокий вакуум, находился свинцовый контейнер с радиоактивным элементом, испускавшим a-частицы. Узкий пучок частиц падал перпендикулярно на поверхность металлической (золотой) фольги, толщиной около 1 мкм (10-6м). Регистрация частиц производилась по вспышкам света (сцинтилляциям), вызываемыми ими на экране, покрытом люминофором. Экран был укреплен перед объективом на корпусе микроскопа, с помощью которого визуально наблюдали сцинтилляции и подсчитывали их число. Так определяли количество частиц, движущихся по данному направлению после их взаимодействия с атомами вещества. Микроскоп вместе с экраном мог вращаться вокруг вертикальной оси, походящей через центр камеры, для регистрации рассеянных атомами фольги частиц.
(рис.1)
На рисунке: 1- атом золота, 2- a-частицы
Более наглядная схема опыта Резерфорда
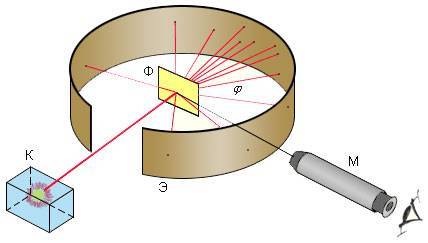
Схема опыта Резерфорда по рассеянию α-частиц.
K – свинцовый контейнер с радиоактивным веществом,Э – экран, покрытый сернистым цинком,Ф – золотая фольга, M – микроскоп.
Результаты опытов Резерфорда:
1.большинство частиц проходит через атомы вещества. не рассеиваясь (как через “пустоту”); 2.с увеличением угла рассеяния число отклонившихся от первоначального направления частиц резко уменьшается; 3.имеются отдельные частицы, отбрасываемые атомами назад, против их первоначального движения (как мяч от стенки).
Резерфорд вывел формулу, по которой можно рассчитать количество a-частиц, рассеянных под определенными углами. В эту формулу входит характеристический параметр “d “, являющийся поперечным размером образований, отклоняющих частицы. Для совпадения расчетов с результатами опытов это параметр должен быть порядка 10-13 см. Атомы имеют диаметр 10-8 см, т.е. на пять порядков выше. Следовательно, в атоме имеется область занимающая ничтожно малую часть атома, которая и отклоняет частицы на большие углы вплоть до 180.
Изучение явления радиоактивности
После открытия радиоактивных элементов началось активное изучение физической природы их излучения. Резерфорду удалось обнаружить сложный состав радиоактивного излучения.
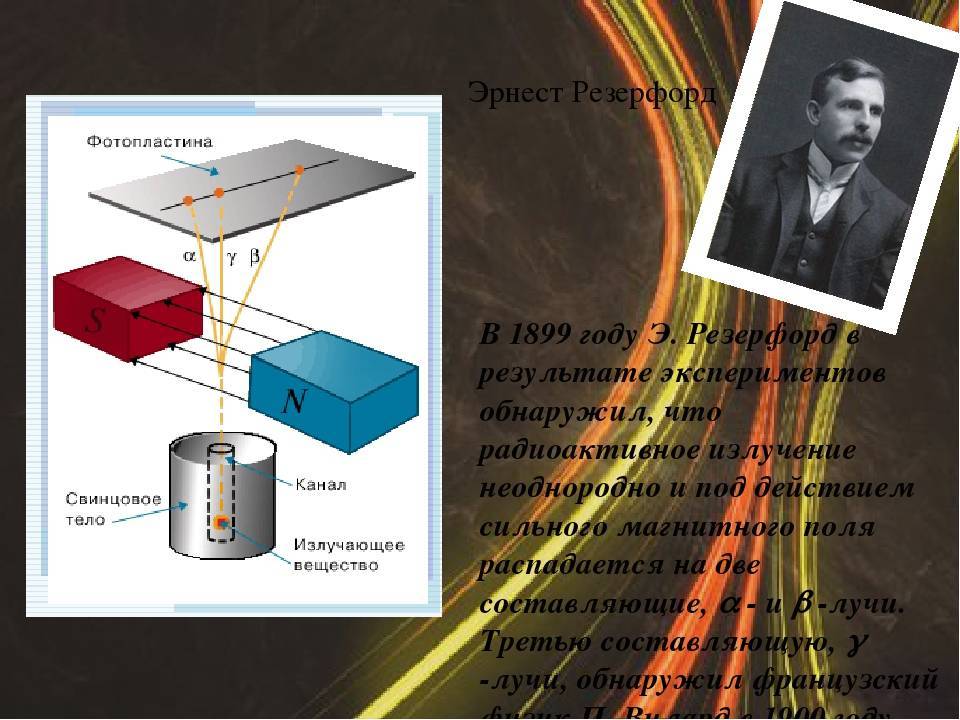
Опыт состоял в следующем. Радиоактивный препарат помещали на дно узкого канала свинцового цилиндра, напротив помещалась фотопластинка. На выходившее из канала излучение действовало магнитное поле. При этом вся установка находилась в вакууме.
В магнитном поле пучок распадался на три части. Две составляющие первичного излучения отклонялись в противоположные стороны, что указывало на наличие у них зарядов противоположных знаков. Третья составляющая сохраняла прямолинейность распространения. Излучение, обладающее положительным зарядом, получило название альфа-лучи, отрицательным — бета-лучи, нейтральным — гамма-лучи.
Изучая природу альфа-излучения, Резерфорд провёл следующий эксперимент. На пути альфа-частиц он поместил счётчик Гейгера , который измерял число испускающихся частиц за определённое время. После этого при помощи электрометра он измерил заряд частиц, испущенных за это же время. Зная суммарный заряд альфа-частиц и их количество, Резерфорд рассчитал заряд одной такой частицы. Он оказался равен двум элементарным.
По отклонению частиц в магнитом поле он определил отношение её заряда к массе. Оказалось, что на один элементарный заряд приходятся две атомные единицы массы.
Таким образом, было установлено, что при заряде, равном двум элементарным, альфа-частица имеет четыре атомные единицы массы. Из этого следует, что альфа-излучение — это поток ядер гелия.
В 1920 году Резерфорд высказал предположение, что должна существовать частица массой, равной массе протона, но не имеющая электрического заряда — нейтрон. Однако обнаружить такую частицу ему не удалось. Её существование было экспериментально доказано Джеймсом Чедвиком в 1932 году.
Кроме того, Резерфорд уточнил на 30 % отношение заряда электрона к его массе.
Cмepть
Эрнест Резерфорд страдал пупочной грыжей, и оперировать его, в знак особой чести (как носителю британского ордена «За заслуги»), надлежало только титулованному хирургу. Из-за долгих поисков подходящей кандидатуры, время было упущено, и 19 октября 1937 г. в больнице Резерфорд внезапно скончался.
Оценка по биографии
Новая функция! Средняя оценка, которую получила эта биография. Показать оценкуСредняя оценка: 5 баллов. Всего получено оценок: 8.
- Уроки
- Тесты по алгебре
- Задать вопрос
- Уроки
- Тесты по английскому языку
- Задать вопрос
Уроки
- 5 класс
- 6 класс
- 7 класс
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по биологии
- Задать вопрос
Уроки
- 5 класс
- 6 класс
- 7 класс
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по истории
- Задать вопрос
Уроки
- 5 класс
- 6 класс
- 7 класс
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по географии
- Задать вопрос
- Презентации по географии
- Тесты по геометрии
- Задать вопрос
Уроки
- 6 класс
- 7 класс
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по истории России
- Задать вопрос
- Биографии
- Краткие содержания
- Анализ стихотворений
- Анализ произведений
- Сочинения
- Библиотека
- Тесты по литературе
- Задать вопрос
- Тесты по математике
- Задать вопрос
Уроки
- 5 класс
- 6 класс
- 7 класс
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по обществознанию
- Задать вопрос
Уроки
- 1 класс
- 2 класс
- 3 класс
- 4 класс
- Тесты по окружающему миру
- Задать вопрос
Уроки
- 2 класс
- 3 класс
- 4 класс
- 5 класс
- 6 класс
- 7 класс
- 8 класс
- 9 класс
- 10 класс
Словари и справочники
- Словарь ударений
- Орфографические трудности
- Морфологический разбор слов
- Фонетический разбор слов
- Корень слова
- Проверочное слово
- Как выделить запятыми
- Тесты по русскому языку
- Задать вопрос
Уроки
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по химии
- Задать вопрос
Уроки
- 7 класс
- 8 класс
- 9 класс
- 10 класс
- 11 класс
- Тесты по физике
- Задать вопрос
- Тесты по чтению
- Задать вопрос
- Помощь с д/з
- Все тесты
- Викторина на 1000 руб.
- Онлайн-батл
- Презентации
- Контакты
- Вход
- Регистрация
Полное или частичное копирование материалов разрешается только с указанием активной гиперссылки на https://obrazovaka.ru
Copyright 2008-2019 Образовака Контакты
Возвращение в Кембридж
Ядерные реакции занимали ученого на протяжении всей карьеры, которая проходила снова в Кембридже, где в 1919 г. преемником Томсона на посту директора Кавендишской лаборатории университета и стал Резерфорд. Эрнест привел сюда своего коллегу по университету Манчестера – физика Джеймса Чедвика. Вместе они бомбардировали альфа-частицами ряд легких элементов и вызывали ядерные превращения. Но им не удавалось проникнуть в более тяжелые ядра, поскольку α-частицы отталкивались от них из-за одинакового заряда, и ученые не могли определить, происходило это раздельно или вместе с мишенью. В обоих случаях требовалась более передовая технология.
Более высокие энергии в ускорителях частиц, необходимые для решения первой проблемы, стали доступны в конце 1920-х годов. В 1932 г. два студента Резерфорда – англичанин Джон Кокрофт и ирландец Эрнест Уолтон – стали первыми, кто фактически вызвал ядерное превращение. С помощью высоковольтного линейного ускорителя они бомбардировали литий протонами и расщепили его на две α-частицы. За эту работу они получили Нобелевскую премию 1951 г. по физике. Шотландец Чарльз Вильсон в Кавендише создал туманную камеру, которая давала визуальное подтверждение траектории заряженных частиц, за что был удостоен этой же престижной международной награды в 1927 г. В 1924-м английский физик Патрик Блэкетт модифицировал камеру Вильсона, чтобы сфотографировать около 400 000 альфа-столкновений и обнаружил, что большинство из них были обычными упругими, а 8 сопровождались распадом, в котором α-частица поглощалась ядром-мишенью перед его расщеплением на два фрагмента. Это стало важным шагом в понимании ядерных реакций, за что Блэкетту была присвоена Нобелевская премия по физике 1948 года.
Личная жизнь
В 1900 году на небольшой срок Эрнест Резерфорд поехал в Новую Зеландию и неожиданно для себя полюбил некую Мэри Джорджину Ньютон, которой впоследствии даже сделал предложение. Она была дочкой хозяйки частного пансиона, в котором он проживал. Они поженились, и 30 марта 1901 г. у счастливый мужа и жены на свет появилась их единственная дочь – Эйлин Мэри. Она вышла замуж за известного астрофизика Ральфа Фаулера и скончалась в 29 лет. Практически до смерти Резерфорд был совершенно здоров и умер в Кембридже в 1937г. впоследствии недолгой неожиданной болезни.Его похоронили рядом с могилами Чарльза Дарвина и Исаака Ньютона.
Сотрудничество с Нильсом Бором
Тем временем планетарная модель занимала его мысли все сильнее. И вот в марте 1912 года Резерфорд стал сотрудничать и дружить с Нильсом Бором. Величайшая заслуга Бора состояла в том, что он внес принципиально новые черты в планетарную модель – идею квантов. Он выдвинул “постулаты”, казавшиеся на первый взгляд внутренне противоречивыми. По его мнению, в атоме есть орбиты. Электрон, двигаясь по ним, не излучает, вопреки законам электродинамики, хотя и имеет ускорение. Этот ученый указал правило, с помощью которого можно найти эти орбиты. Он выяснил, что кванты излучения появляются лишь при переходе электрона с орбиты на орбиту. Модель атома Резерфорда-Бора решила многие проблемы, а также стала прорывом в мир новых идей. Ее открытие привело к коренному пересмотру представлений о материи, о ее движении.
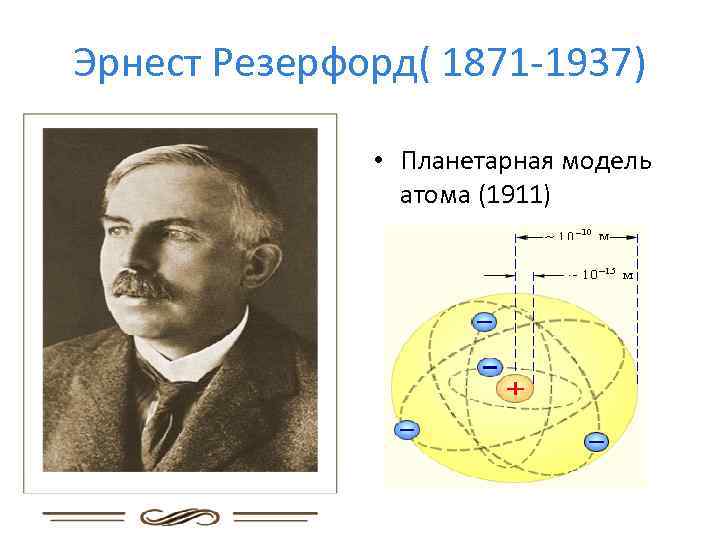
Планетарная модель Резерфорда
И тогда вновь проявилась интуиция Резерфорда и умение этого ученого понимать язык природы. Эрнест решительно отказался от предложенной Томсоном модели атома. Опыты Резерфорда привели к тому, что он выдвинул свою, получившую название планетарной. Согласно ей, в центре атома находится ядро, в котором сосредоточена вся масса данного атома, несмотря на его довольно малые размеры. А вокруг ядра, подобно планетам, вращающимся вокруг Солнца, движутся электроны. Массы их существенно меньше, чем у альфа-частиц, и именно поэтому последние практически не отклоняются, когда пронизывают электронные облака. И лишь когда близко от ядра, положительно заряженного, пролетает альфа-частица, кулоновская сила отталкивания способна резко искривить траекторию ее движения. Такова теория Резерфорда.
Безусловно, это было великое открытие. Законы электродинамики и планетарная модель Опыта Резерфорда было достаточно для того, чтобы убедить многих ученых в существовании планетарной модели. Однако выяснилось, что она не так однозначна. Формула Резерфорда, которую он вывел с опорой на эту модель, согласовалась с данными, полученными в ходе эксперимента. Однако она опровергала законы электродинамики!
Законы эти, которые были установлены в основном трудами Максвелла и Фарадея, утверждают, что заряд, ускоренно движущийся, излучает электромагнитные волны и теряет из-за этого энергию. В атоме Резерфорда электрон движется в кулоновском поле ядра ускоренно и, согласно теории Максвелла, он должен потерять всю энергию за десятимиллионную долю секунды, после чего упасть на ядро. Однако этого не происходило. Следовательно, формула Резерфорда опровергала теорию Максвелла. Эрнест знал об этом, когда в 1907 году настало время возвращаться в Англию.
Исследования и открытия
В 1895 году, будучи первым студентом-исследователем в Университете Кембриджа Лаборатория Кавендиша в Лондоне, Резерфорд, определила более простое и коммерчески жизнеспособное средство обнаружения радиоволн, чем ранее созданный немецким физиком Генрихом Герцем.
Также в лаборатории Кавендиша профессор Дж. Томсон пригласил Резерфорда принять участие в исследовании рентгеновских лучей. Немецкий физик Вильгельм Конрад Рентген открыл рентгеновские лучи всего за несколько месяцев до прибытия Резерфорда в Кавендиш, и рентгеновские лучи были горячей темой среди ученых-исследователей. Вместе Резерфорд и Томсон изучили влияние рентгеновских лучей на проводимость газов, в результате чего появилась статья о разделении атомов и молекул на ионы. В то время как Томсон продолжал исследовать то, что позже будет называться электроном, Резерфорд более внимательно изучил излучение, генерирующее ионы.
Сосредоточившись на уране, Резерфорд обнаружил, что размещение его вблизи фольги приводит к тому, что один тип излучения является легко впитывается или блокируется, в то время как другой тип без проблем проникает в ту же фольгу. Он обозначил два типа излучения: альфа и бета. Как оказалось, альфа-частица была идентична ядру атома гелия. Фактически, бета-частица была такой же, как электрон или позитрон.
Резерфорд покинул Кембридж в 1902 году и стал профессором в университете Макгилла в Монреале. В McGill в 1903 году Резерфорд и его коллега Фредерик Содди представили свою теорию радиоактивности распада, которая утверждала, что радиоактивная энергия испускалась изнутри атома и что, когда альфа- и бета-частицы испускались одновременно, они вызывали химические изменения в элементах. Резерфорд и Йельский профессор Бертрам Борден Болтвуд продолжили классифицировать радиоактивные элементы в так называемую серию распада Резерфорду также приписывают открытие радиоактивного газового радона в Макгилле.Добившись известности за его вклад в понимание радиоэлементов, Резерфорд стал активным публичным оратором, опубликовал множество журнальных статей и написал самый уважаемый учебник того времени по радиоактивности.
В 1907 году Резерфорд вернулся в Англию, переведя до профессора в университете Манчестера. Путем дальнейших экспериментов с использованием альфа-частиц в фольге Резерфорд сделал потрясающее открытие, что почти вся масса атома сосредоточена в ядре. При этом он породил ядерную модель, открытие, которое ознаменовало зарождение ядерной физики и в конечном итоге проложило путь к изобретению атомной бомбы. Удачно названный «Отцом ядерного века», Резерфорд получил Нобелевскую премию по химии в 1908 году.
С началом Первой мировой войны Резерфорд обратил свое внимание на противолодочные исследования. К 1919 году он сделал еще одно монументальное открытие: как искусственно вызвать ядерную реакцию в стабильном элементе
Ядерные реакции были основным направлением деятельности Резерфорда до конца его научной карьеры.
Кембридж
В знак признания растущей важности науки Кембриджский университет изменил свои правила, позволив выпускникам других вузов получать диплом после двух лет обучения и выполнения приемлемой научной работы. Первым студентом-исследователем стал Резерфорд
Эрнест, кроме демонстрации намагничивания колебательным разрядом железа, установил, что игла теряет часть своей намагниченности в магнитном поле, создаваемом переменным током. Это позволило создать детектор недавно открытых электромагнитных волн. В 1864 г. шотландский физик-теоретик Джеймс Клерк Максвелл предсказал их существование, а в 1885–1889 гг. немецкий физик Генрих Герц обнаружил их в своей лаборатории. Прибор Резерфорда для детекции радиоволн был проще и имел коммерческий потенциал. Следующий год молодой ученый провел в Кавендишской лаборатории, увеличивая диапазон и чувствительность прибора, который мог принимать сигналы на расстоянии полумили. Однако Резерфорду не хватило межконтинентального видения и предпринимательских навыков итальянца Гульельмо Маркони, который изобрел беспроводной телеграф в 1896 г.

Дальнейшая обширная деятельность
В 1919 году Резерфорд стал профессором Кембриджского университета, а также директором Кавендишевской лаборатории. Десятки ученых справедливо считали его своим учителем, включая впоследствии удостоенных Нобелевских премий. Это Дж. Чедвик, Г. Мозли, М. Олифант, Дж. Кокрофт, О. Ган, В. Гейтлер, Ю.Б. Харитон, П.Л. Капица, Г. Гамов и др.
Поток почестей и наград становился все обильнее.
В 1914 году Резерфорд получает дворянство.
Президентом Британской ассоциации он становится в 1923 году, а с 1925 по 1930 являлся президентом Королевского общества.
Титул барона Эрнест получает в 1931 году и становится лордом. Однако, несмотря на все более высокие нагрузки, и не только научные, он продолжает атаки на тайны ядра и атома.
Предлагаем вам один интересный факт, связанный с научной деятельностью Резерфорда. Известно, что Эрнест Резерфорд пользовался следующим критерием, когда выбирал себе сотрудников: он давал человеку, пришедшему к нему впервые, задание, и если новый сотрудник после этого интересовался, что ему делать дальше, его сразу же увольняли.
Ученый уже приступил к экспериментам, которые окончились открытием им искусственного расщепления ядер атомов и искусственного превращения химических элементов.
В 1920 году Резерфорд предсказал существование дейтрона и нейтрона, а в 1933 стал инициатором и участником эксперимента по проверке существующей в ядерных процессах взаимосвязи энергии и массы.
В 1932 году, в апреле, он поддержал идею применения ускорителей протонов при исследовании ядерных реакций.
Детство и юность
Эрнест родился в Новой Зеландии, в Спринг-Груве, рядом с городом Нелсон 30 августа 1871 года и был британцем по национальности. Отец, шотландец по происхождению, зарабатывал колесным ремеслом, а мать преподавала в сельской школе. Ребенок рос в многодетной семье с 6 братьями и 5 сестрами.
Первым рабочим местом для него стало деревообрабатывающее предприятие, основанное отцом. Полученные в детстве знания и навыки будущий ученый использовал в дальнейшем для создания оборудования, необходимого при физических опытах.
 Памятник Эрнесту Резерфорду в детстве / Alan Liefting, Википедия
Памятник Эрнесту Резерфорду в детстве / Alan Liefting, Википедия
Эрнест учился в Хавелоке, а в 1887-м получил стипендию, позволившую продолжить образование в Нелсоне. Юноша демонстрировал большую тягу к знаниям и интерес ко всему, что его окружает. Он поступил в Кентерберийский колледж и начал углубляться в химию и физику. Педагоги быстро оценили потенциал ученика. Через 4 года Резерфорда наградили за лучшую работу по математике и физике. В 1892-м Эрнест стал магистром искусств и занялся исследованиями, подкрепляя их опытами.
Его первый труд называется «Магнетизация железа при высокочастотных разрядах». Эксперименты были связаны с исследованием высокочастотных радиоволн. Ученый сконструировал радиоприемник, опередив его официального создателя Маркони. Устройство Резерфорда оказалось первым в мире магнитным детектором.
 Эрнест Резерфорд в молодости / Википедия
Эрнест Резерфорд в молодости / Википедия
С его помощью Эрнест получал сигналы, которые коллеги передавали, находясь в полумиле от него. Полученные сведения он описал в научной статье для газеты «Известия философского института Новой Зеландии» в 1894 году.
В 1895-м Резерфорд получил высочайшую награду: грант на обучение в Великобритании. Такой шанс выпадал редкому английскому подданному. Эрнест оказался в числе 2 счастливчиков, между которыми предстояло сделать выбор, и ему повезло: соперник не смог отправиться в поездку. Физик воспользовался возможностью и стал в Англии сотрудником Кавендишевской лаборатории.
Труды, исследования и вклад в науку
В 1898 г. Резерфорд меняет Хью Лонгборна Каллендара на должности профессора физики, основанной благодаря покровительству Уильяма МакДональда, в Университете МакГилла. Именно здесь Резерфорд достигнет высот своей исследовательской деятельности. Его работа в Университете МакГилла увенчается получением в 1908 г. Нобелевской премии в области химии.
Резерфорд занимается глубинными исследованиями и практическим изучением явления радиоактивности. В этот период, в 1899 г., он вводит понятия альфа- и бета-частиц. Этот тип радиационного излучения учёный описывает как два отчётливых (легко различаемых) вида излучения потока частиц элементами торием и ураном. Основываясь на их проникающей способности, Резерфорд чётко излагает различия этих радиационных лучей.
В 1900 г. в Университете Новой Зеландии он получает степень доктора наук. С 1900 г. по 1903 г. к исследовательскому проекту Резерфорда на тему трансмутации элементов в Университете МакГилла присоединяется юный исследователь Фредерик Содди.
Резерфорд открывает и точно описывает, что радиация является следствием спонтанного разложения атомов. Учёный в мельчайших подробностях наблюдает, а в последствие и описывает, что образцу радиоактивного материала требуется определенное время для уменьшения его радиоактивности в 2 раза. Это время Резерфорд называет «периодом полураспада». Это открытие в дальнейшем получит практическое применение: взяв за единицу измерения равномерную скорость распада вещества, будет определён возраста планеты Земля, оказавшейся намного старше, чем возраст, предполагаемый учёными того времени.
В 1903 г. Резерфорд обнаруживает, что радиация (уже открытая), излучаемая ещё безымянным радием (открытым в 1900 г. французским химиком Полом Виллардом) обладает отличительной чертой (от альфа- и бета-излучений), не описанной прежде. Он также замечает, что новый вид излучения обладает большой проникающей способность, и, не теряя времени, даёт ему самостоятельное название «гамма-излучение». В 1907 г. Резерфорда назначают на должность профессора физики Манчестерского университета. В Манчестере учёный продолжает работать с альфа-излучением. Совместно с Гансом Гейгером, он разрабатывает цинк-сульфидный отражающий экран и ионизационную камеру, предназначенную для подсчёта количества альфа-частиц.
В 1907 г. Резерфорд, вместе с Томасом Ройдсом, проводит химический опыт, заключающийся в прохождении альфа-лучей через узкое окно в вакуумную трубку. Лучи неизменно порождают в трубке искровой разряд, в результате чего образовывается спектр, меняющий свою природу аналогично альфа-лучам, накопившимся в трубке. Далее эксперимент показывает, как начинает образовываться чистый спектр газа гелия. Из этого следует, что альфа-лучи почти не ионизируют атомы, а точнее – ядра атомов, гелия.
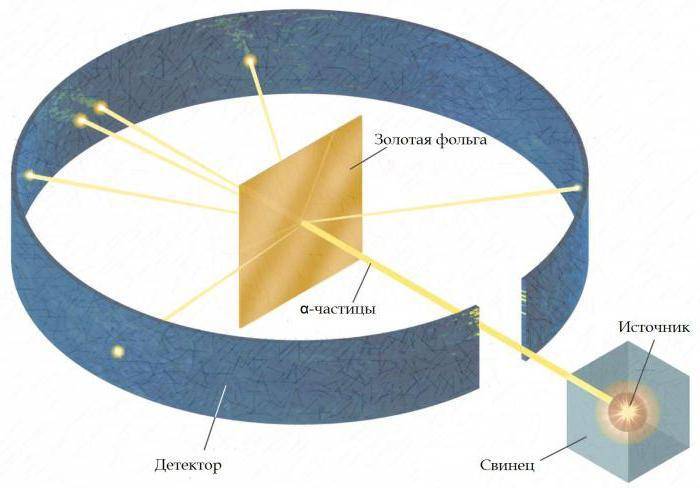
В 1909 г. объединяет усилия с Гансом Гейгером и Эрнестом Марсденом и проводит опыт Гейгера-Марсдена, нацеленный на обнаружение и наглядную демонстрацию истинной ядерной природы атомов. Эксперимент проводится для получения чётко сформулированных результатов относительно свойств альфа-частиц. Резерфорд предлагает Гейгеру и Марсдену получить отклонение альфа-частиц на большие углы (предрешённых результатов опыта не было, поскольку, на момент его проведения, не существовало ни малейших теорий на этот счёт). Искомые отклонения были найдены, но носили единичный характер и ровную, чётко-организованную функцию угла отклонения. Истолкование и результаты этого эксперимента в 1911 г. выливаются в представление модели атома Резерфорда. Согласно его теории, даже маленькое положительно заряженное ядро имеет вращающиеся вокруг него электроны. В 1919 г. Резерфорд отправляется в Кавендишскую лабораторию, где проводит (первым в истории) опыт по трансмутации одного вещества в другое, превратив с помощью ядерной реакции азот в кислород. Этот опыт он осуществляет совместно с Нильсом Бором, выдвигая при этом теорию о существовании нейтронов и об их предположительном свойстве возмещать отталкивающее свойство положительно заряженных протонов, порождая силу ядерного притяжения, удерживающую ядро от распада.
В 1932 г. эту теорию существования нейтронов доказывает Джеймс Чедвик, получивший в 1935 г. Нобелевскую премию в области физики за это открытие.
Университет Манчестера
В Северной Америке было хорошее научное сообщество, но мировой центр физики находился в Европе. Эрнест Резерфорд, Нобелевская премия по химии которому за его работу в Монреале была присуждена в 1908 г., годом ранее устроился на кафедру университета Манчестера, чья лаборатория уступала только Кавендишской.
Совместно с немецким физиком Гансом Гейгером Эрнест Резерфорд создал электрический счетчик ионизированных частиц. Усовершенствованный Гейгером, счетчик стал универсальным инструментом для измерения радиоактивности. Благодаря мастерству стеклодува Резерфорд и его ученик Томас Ройдс выделили некоторые α-частицы и выполнили их спектрохимический анализ, который доказал, что они являются ионами гелия. Затем Болтвуд посетил лабораторию университета Манчестера, и вместе с новозеландским физиком они уточнили скорость образования гелия из радия, из которой они вычислили точное значение числа Авогадро.
Не оставляя своего давнего увлечения альфа-частицами, Резерфорд изучал их небольшое рассеяние после взаимодействия с фольгой. Гейгер присоединился к нему, и они получили больше значимых данных. В 1909 г., когда студент-старшекурсник Эрнест Марсден искал тему для своего научно-исследовательского проекта, Эрнест предложил ему изучить большие углы рассеяния. Марсден обнаружил, что небольшое число α-частиц отклонялось более чем на 90° от своего первоначального направления, что вынудило Резерфорда воскликнуть, что это почти так же невероятно, как если бы 15-дюймовый снаряд, запущенный в лист папиросной бумаги, отскочил бы обратно и попал в стрелявшего.
Научная деятельность
Согласно воспоминаниям П. Л. Капицы, Резерфорд был ярким представителем английской экспериментальной школы в физике, которая характерна стремлением разобраться в сути физического явления и проверить, может ли оно быть объяснено существующими теориями (в отличие от «немецкой» школы экспериментаторов, которая исходит из существующих теорий и стремится проверить их опытом). Он мало пользовался формулами и мало прибегал к математике, но был гениальным экспериментатором, напоминая в этом отношении Фарадея. Отмечаемым Капицей важным качеством Резерфорда как экспериментатора была его наблюдательность. В частности, благодаря ей он открыл эманацию тория, заметив различия в показаниях электроскопа, измерявшего ионизацию, при открытой и закрытой дверце в приборе, перекрывавшей поток воздуха. Другой пример — открытие Резерфордом искусственной трансмутации элементов, когда облучение ядер азота в воздухе альфа-частицами сопровождалось появлением высокоэнергичных частиц (протонов), имевших больший пробег, но очень редких.
Резерфорд написал и опубликовал три тома работ. Все они носят экспериментальный характер.
1904 год — «Радиоактивность».
1905 год — «Радиоактивные превращения».
1930 год — «Излучения радиоактивных веществ» (в соавторстве с Дж. Чедвиком и Ч. Эллисом).
12 учеников Резерфорда стали лауреатами Нобелевской премии по физике и химии. Один из наиболее талантливых учеников Генри Мозли, экспериментально показавший физический смысл Периодического закона, погиб в 1915 году на Галлиполи в ходе Дарданелльской операции. В Монреале Резерфорд работал с Ф. Содди, О. Ханом; в Манчестере — с Г. Гейгером (в частности, помог тому разработать счётчик для автоматического подсчёта числа ионизирующих частиц), в Кембридже — с Н. Бором, П. Капицей и многими другими знаменитыми в будущем учёными.
Теория превращений
Резерфорду потребовалась помощь эксперта-химика, чтобы справиться с ростом числа радиоактивных элементов. Он привлек Фредерика Содди из Макгилла, Бертрама Бордена Болтвуда, профессора Йельского университета, и Отто Гана, научного сотрудника из Германии. С Содди в 1902–1903 гг. он разработал теорию преобразований, объясняющую явление радиоактивности. Алхимия с ее попытками превращения свинца в золото давно была изгнана из современной химии. Атомы считались стабильными. Но Резерфорд и Содди утверждали, что энергия радиоактивности исходит из них, и спонтанное испускание α- или β-частиц означает химическое превращение одного элемента в другой. Они ожидали, что эта иконоборческая теория будет опровергаться, но авторитет множества экспериментальных доказательств подавил оппозицию.
Вскоре было установлено, что радиоактивные элементы делятся на три ряда, возглавляемые ураном, торием и актинием, и все они ведут к образованию неактивного свинца. Болтвуд поместил радий в группу урана и, следуя совету Резерфорда, использовал медленно растущее количество свинца в минерале, чтобы показать, что возраст пород исчисляется миллиардами лет. Последний считал, что альфа-частица, обладающая ощутимой массой, играет ключевую роль в преобразовании элементов. Он определил, что она несет положительный заряд, но не смог установить, является ли она ионом водорода или гелия.
Резерфорд отправляется в Англию
Самым одаренным молодым подданным английской короны из Новой Зеландии предоставлялась раз в два года стипендия им. Всемирной выставки 1851 года, которая давала возможность отправиться в Англию для изучения наук. В 1895 году решено было, что два новозеландца достойны такой чести – физик Резерфорд и химик Маклорен. Однако место было только одно, и надежды Эрнеста рухнули. К счастью, Маклорен вынужден был по семейным обстоятельствам отказаться от этой поездки, и Резерфорд Эрнест осенью 1895 года прибыл в Англию. Здесь он начал работу в Кембриджском университете (в Кавендишевской лаборатории) и стал первым докторантом Дж. Томсона, ее директора (на фото ниже).
Модель атома
Размышляя над тем, как такая тяжелая заряженная частица может отклоняться электростатическим притяжением или отталкиванием на такой большой угол, в 1944 г. Резерфорд пришел к выводу, что атом не может являться однородным твердым телом. По его мнению, он состоял в основном из пустого пространства и крошечного ядра, в котором сконцентрирована вся его масса. Резерфорд Эрнест модель атома подтвердил многочисленными экспериментальными доказательствами. Она стала его наибольшим научным вкладом, но за пределами Манчестера на нее обращали мало внимания
В 1913 г., однако, датский физик Нильс Бор показал всю важность этого открытия. Годом ранее он посетил лабораторию Резерфорда и вернулся в нее в качестве сотрудника факультета в 1914–1916 гг
Радиоактивность, как объяснил он, заключена в ядре, в то время как химические свойства определяются орбитальными электронами. Модель атома Бора породила новую концепцию квантов (или дискретных значений энергии) в электродинамике орбит, и он объяснил спектральные линии как выделение или поглощение энергии электронами при их переходе из одной орбиты на другую. Генри Мозли, еще один из многих учеников Резерфорда, аналогичным образом объяснил последовательность рентгеновского спектра элементов зарядом ядра. Таким образом была разработана новая согласованная картина физики атома.
Открытие закона радиоактивных превращений
Вокруг Резерфорда уже тогда сформировалась атмосфера творческого энтузиазма и увлеченности. Труд был радостным и напряженным, он приводил к большим успехам. Резерфорд в 1899 году открыл эманацию тория. Совместно с Содди в 1902-1903 годах он пришел уже к общему закону, применимому ко всем радиоактивным превращениям
Следует сказать несколько подробнее об этом важном научном событии
Ученые всего мира твердо усвоили в то время, что невозможно превратить одни химические элементы в другие, поэтому следует навеки похоронить мечты алхимиков добывать из свинца золото. И вот появилась работа, в которой утверждалось, что при радиоактивных распадах превращения элементов не только происходят, но их невозможно ни замедлить, ни прекратить. Более того, были сформулированы законы этих превращений.
Сегодня мы понимаем, что именно зарядом ядра определяются химические свойства элемента и его положение в периодической системе Менделеева. Когда на две единицы уменьшается заряд ядра, что происходит при альфа-распаде, он “перемещается” вверх на 2 клеточки в таблице Менделеева. На одну клетку вниз он смещается при электронном бета-распаде, а на клетку вверх – при позитронном. Несмотря на очевидность этого закона и его кажущуюся простоту, это открытие было одним из самых важных событий в науке начала 20 века.